§ 23.
ТЕМПЕРАТУРА, ТЕПЛОВОЕ РАВНОВЕСИЕ, АБСОЛЮТНАЯ ТЕМПЕРАТУРА.
Тепловое равновесие между телами возможно только
тогда, когда их температура одинакова.
Прикоснувшись рукой к
любому предмету, мы легко можем определить, тёплый он или холодный. Если температура
предмета ниже температуры руки, предмет кажется холодным, а если наоборот, то -
тёплым. Если зажать в кулаке холодную монету, то теплота руки начнёт нагревать
монету, и через некоторое время её температура станет равной температуре руки,
или, как говорят, наступит тепловое равновесие. Поэтому температура
характеризует состояние теплового равновесия системы из двух или нескольких
тел, имеющих одну и ту же температуру. Так, говоря, что температура нашего тела
равна 36 оС, мы подразумеваем, что градусник подмышкой
находится в тепловом равновесии с окружающими тканями, когда он показывает 36
оС.
Температура наряду с
объёмом и давлением газа являются макроскопическими параметрами. Для
измерения температуры используют термометры. В некоторых из них регистрируют
изменение объёма жидкости при нагревании, в других – изменение электрического
сопротивления и т.п. Самой распространённой является температурная шкала Цельсия,
названная так в честь шведского физика А. Цельсия. Чтобы получить температурную
шкалу Цельсия для жидкостного термометра, его сначала погружают в тающий лёд и
отмечают положение конца столбика, а потом - в кипящую воду. Отрезок между
этими двумя положениями столбика делят на 100 равных частей, считая, что
температура таяния льда соответствует нулю градусов шкалы Цельсия (оС),
а температура кипящей воды – 100 оС (см. рис. 23а).
Основное уравнение
молекулярно-кинетической теории (22.4) связывает между собой давление газа,
концентрацию молекул и их среднюю кинетическую энергию. Однако средняя
кинетическая энергия молекул, как правило, неизвестна, хотя результаты многих
опытов говорят о том, что скорость молекул увеличивается с ростом температуры
(см., например, броуновское движение в §20). Зависимость средней кинетической
энергии молекул газа от его температуры можно получить из закона открытого
французским физиком Ж. Шарлем в 1787 году.
Согласно закону Шарля,
если объём данной массы газа не меняется, его давление pt линейно зависит от температуры t:
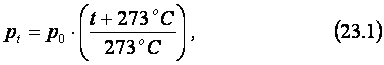
где t – температура газа, измеренная в оС,
а p0
– давление газа при температуре 0 оС (см. рис. 23б).
Таким образом, из закона Шарля следует, что давление газа, занимающего неизменный
объём, пропорционально сумме (t+273 оС). С другой стороны, из (22.4)
вытекает, что, если концентрация молекул постоянна, т.е. объём, занимаемый
газом, не изменяется, то давление газа должно быть пропорционально средней
кинетической энергии молекул. Значит, средняя кинетическая энергия, ЕСР молекул газа, просто,
пропорциональна величине (t+273 оС):
![]()
где b – постоянный коэффициент, значение
которого мы позже определим. Из (23.2) следует, что средняя кинетическая
энергия молекул станет равной нулю при -273 оС. Исходя из
этого, английский учёный У. Кельвин в 1848 г. предложил использовать абсолютную
температурную шкалу, нулевая температура в которой соответствовала бы -273
оС, а каждый градус температуры был бы равен градусу шкалы
Цельсия. Таким образом, абсолютная температура, T связана с температурой t, измеренной по шкале Цельсия,
следующим образом:
![]()
За
единицу абсолютной температуры в СИ принят Кельвин (К).
Учитывая (23.3),
уравнение (23.2) преобразуется в:
![]()
подставляя
которое в (22.4), получаем следующее:

Чтобы
избавиться от дроби в (23.5), заменим 2b/3 на k, и получим вместо (23.4) и (23.5)
два очень важных уравнения:

где k – постоянная Больцмана,
названная в честь Л. Больцмана. Эксперименты показали, что k=1,38.10-23 Дж/К. Таким образом, давление газа и средняя кинетическая
энергия его молекул пропорциональны его абсолютной температуре.
Вопросы для
повторения:
·
Как связана температура с тепловым равновесием?
·
Сформулируйте закон Шарля.
·
При какой температуре прекращается тепловое движение?
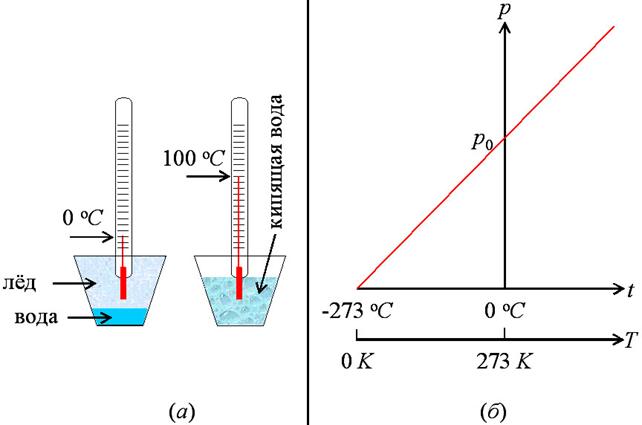
Рис. 23.
(а) – градуировка термометра по шкале Цельсия; (б) – графическое
представление закона Шарля.