§ 32. НЕОБРАТИМОСТЬ ТЕПЛОВЫХ
ПРОЦЕССОВ. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ.
Процессы в природе необратимы, а их направление
подчиняется общей закономерности – более упорядоченные состояния замкнутых
систем переходят в менее упорядоченные.
Если лежащий на земле мяч
слегка толкнуть ногой, то он, прокатившись по земле, остановится, а вся его
кинетическая энергия перейдёт в тепловую, в результате
чего он сам и участки земли, которых он касался, станут чуть теплее. Другими
словами, вся кинетическая энергия упорядоченного движения мяча переходит во внутреннюю
энергию хаотического движения молекул. А можно ли сделать наоборот, чтобы часть
энергии хаотического движения молекул перешла в кинетическую энергию его
упорядоченного движения, как целого? В принципе, можно себе представить, что
совершенно случайно все молекулы мяча в своём тепловом движении вдруг начинают
двигаться в одном направлении. Тогда очевидно, что и весь мяч двинется в ту же
сторону. Интересно, что такая случайная координация между движениями всех
молекул не противоречит закону сохранения энергии, но жизненный опыт нам
подсказывает, что этого быть не может, т.к. вероятность такого события очень и
очень мала. Таким образом, процесс скольжения мяча является необратимым, при
котором вся кинетическая энергия переходит в тепловую,
а упорядоченное движение заменяется хаотичным.
Можно привести много
примеров необратимости тепловых процессов. Если два тела разной температуры
соприкасаются, то более горячее тело остывает, а более холодное нагревается,
хотя закон сохранения энергии, вообще говоря, не запрещает и обратное. Поэтому теплообмен
между неодинаково нагретыми телами тоже необратим и происходит только от более
нагретого тела к менее нагретому (рис. 32а).
Можно считать, что до начала теплообмена молекулы были расположены упорядоченно
– молекулы с малой кинетической энергией в менее нагретом теле, а молекулы с
большой энергией в более нагретом. Таким образом, как и в случае с катящимся по
полю мячом, теплообмен происходит в направлении от порядка к его отсутствию.
Свойство газа занимать
весь объём сосуда, в котором он находится, тоже возникает из-за стремления
молекул газа к беспорядку. Если сначала разместить все молекулы газа в какой-то
малой части сосуда, а потом снять ограничения, разрешив им двигаться, то они равномерно
заполнят весь его объём (рис. 32б). Как и в предыдущих случаях, вероятность
того, что молекулы опять соберутся все вместе в той части сосуда, где они были
сначала, ничтожно мала. Поэтому и этот процесс расширения газа тоже необратим.
Таким образом, можно
утверждать, что, если замкнутая система из макроскопических тел переходит в
другое состояние, то этот переход необратим, т.к. он всегда происходит из менее
вероятного состояния в более вероятное. Это утверждение называют вторым законом
термодинамики, который указывает направление протекания тепловых процессов
в природе.
Существуют, однако, и
несколько других формулировок второго закона термодинамики. Одна из них
принадлежит немецкому учёному Р. Клаузису – «Невозможен процесс, единственным
результатом которого был бы переход количества теплоты от холодного тела к
горячему». Другими словами, теплообмен в замкнутой системе может происходить
только в одном направлении – от горячего тела к холодному.
Докажем с помощью второго
закона термодинамики в формулировке Клаузиса, что количество теплоты, полученное
при охлаждении какого-либо тела А не может быть
полностью преобразовано в механическую энергию тела Б. Действительно,
если бы это удалось, то тогда можно было бы нагреть любое тело В, более
горячее, чем А, с помощью силы трения, возникающей при движении тела Б
по телу В. В результате, система из тел А,Б и В перешла бы в новое состояние, отличное от старого
только тем, что некоторое количество теплоты перешло от тела А к более
горячему телу В. А такой процесс запрещён вторым законом термодинамики,
и значит, всё количество теплоты не может быть преобразовано в механическую
энергию.
Потребности человеческого
общества в различных видах энергии возрастают с каждым годом. При этом большая
часть электрической и механической энергии производится тепловыми двигателями,
в частности, двигателями внутреннего сгорания, КПД которых ограничен вторым законом
термодинамики и уравнением (31.2). И, чем больше человечество производит
энергии, тем больше оно нагревает окружающую среду и загрязняет её экологически
вредными продуктами сгорания. Поэтому будущее мировой энергетики связано с использованием
энергосберегающих технологий и возобновляемых источников энергии (ветер,
приливы, солнечная энергия и т.п.).
Вопросы для повторения:
·
Приведите примеры необратимых тепловых процессов.
·
Сформулируйте второй закон термодинамики и следствия из него.
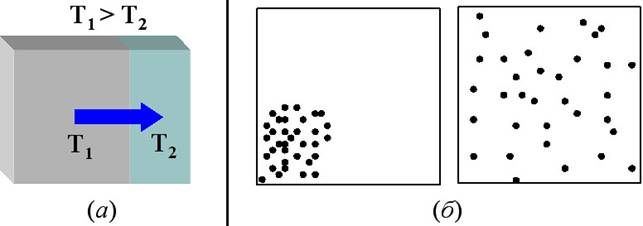
Рис. 32. Иллюстрация необратимости при теплообмене (а, стрелкой
показано направление передачи теплоты) и расширении газа в пустоту (б,
слева – начальное состояние).